2015年6月20日 星期六
MDMA - 5
圖片一:動物實驗發現MDMA會對實驗動物的腦神經細胞造成神經毒性。
( 圖片來源:http://goo.gl/1Mh0Xx )
09
MDMA列為一級管制藥品,意味著使用、持有和販賣皆成為非法行為;能夠合法使用MDMA的途徑,只剩下經由政府單位核准的科學研究。然而,要拿MDMA進行什麼方向的科學研究,其實受到了研究申請程序的重重關卡的限制,特別是進行MDMA的人體試驗研究。由於MDMA屬於一級管制藥品,其定義為沒有醫療用途價值、具高濫用風險、在醫療人員監督下使用仍欠缺安全性,等於是下了結論表示MDMA用在人體上有百害無一利(雖然很明顯地是缺乏證據的),並且在研究倫理的考量下不應讓試驗者承受傷害的高風險,不值得進行研究。在此情況下,研究者若想申請MDMA的人體試驗,無論在研究經費上(政府或私人單位皆然)、研究核准上(需經過FDA和人體試驗委員會(Institutional Review Board, IRB)的同意)勢必都遇到阻礙,而且若要能夠合法取得MDMA,還需要獲得DEA核發的執照來購買、保存與管理研究用MDMA,在在增加了程序和研究成本的負擔。
所以什麼樣的MDMA研究最能夠順利進行?就是企圖證明MDMA毒害性的研究,而這樣的研究會獲得政府大力的經費、資源贊助,以獲得科學證據來鞏固政府將MDMA列為一級管制藥品的合法性。然而,先立法、再證明的程序,豈不是一個顛倒的作為?
因為認定MDMA用在人體上有危害性,不應以人作為試驗者,因此企圖證明MDMA具有毒害性的研究,便由實驗動物先做起。
累積了多年的實驗動物研究(主要是老鼠),科學家發現將高劑量(大於10毫克/每公斤)的MDMA多次(一天內一到四次不等,連續二到四天不等)地經由皮下或腹腔內注射入實驗動物體內後,會有以下的一些發現:
1. 腦部的血清素與血清素之代謝物5-HIAA濃度下降、合成血清素的酵素功能下降,並且會持續一段時
間
2. 分泌血清素的神經細胞軸突末端上,血清素傳輸器的量減少、回收血清素的量也減少
3. 分泌血清素的神經細胞,其較末端的軸突數量會減損,留存的軸突則會出現腫脹和破裂化,稍後增
生的軸突也與原先之神經結構不同
科學家以上述的實驗結果,認定MDMA會造成大腦的血清素系統運作功能遭受到影響,因此判定MDMA具有(血清素)神經毒性(neurotoxicity)。
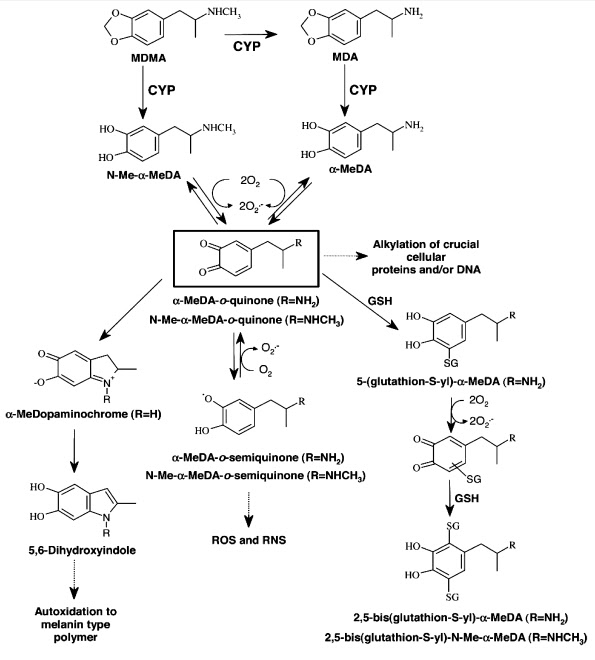
科學家更進一步發現造成神經毒性的不是MDMA,而是MDMA在經過代謝後,會形成具破壞性的過氧化物和自由基分子,而這些過氧化物和自由基分子造成了神經細胞的傷害。此外,MDMA會促使體溫上升,體溫上升會加速MDMA的代謝而讓過氧化物和自由基分子的濃度增加,增加對神經細胞的破壞性。科學家也發現,實驗動物若處在較高的室溫環境,也會提升MDMA的代謝速度、增加MDMA的過氧化物和自由基分子濃度而產生神經毒性。
圖片二:MDMA(左上角)經過肝臟代謝後,會形成過氧化物和自由基分子而造成神經細胞的影響。
( 圖片來源:Green AR, King MV, Shortall SE, Fone KC. Lost in translation: preclinical studies on 3,4-
methylenedioxymethamphetamine provide information on mechanisms of action, but do not allow
accurate prediction of adverse events in humans. Br J Pharmacol. 2012 Jul;166(5):1523-36. )
由於直接將MDMA給予人類試驗者使用,以確認MDMA是否對人類大腦也具有傷害性有違研究倫理的考量,因此MDMA的人類研究大多只能採取「回溯性」的研究法,也就是取樣出「曾經」使用過Ecstasy的人(一般認定MDMA是Ecstasy的主要成分),進行各式的認知功能、神經心理測驗,再與無使用過Ecstasy的人之測驗結果進行分析比較,是否MDMA可能造成人類的神經功能損害。這類的回溯式研究也累積了多年的成果,而許多的研究結果顯示,Ecstasy使用者會在不同的神經功能類別中―包括記憶力、執行功能等等―出現長期的損害,還會增加憂鬱、焦慮和衝動性的症狀表現。而腦部的影像學研究也發現在Ecstasy使用者的特定腦部區域包括海馬迴(掌管記憶功能)和前額葉(掌管判斷和執行功能),由縫核延伸軸突至此的血清素細胞軸突末端,其上面的血清素傳輸器密度較低,研究者因此認定這些腦部特定區域的血清素傳輸器數量的變化,便是造成血清素系統損害的神經毒性證據,足以解釋為什麼Ecstasy使用者會出現記憶力和執行功能的損害。
有了實驗動物直接測試出MDMA對血清素系統之神經毒性,加上人類的Ecstasy使用者之神經功能測驗有減損的佐證,科學證據成為了支持各國政府將MDMA列為管制藥品的重要力量。
然而,這些研究真的辨認清楚了MDMA的面貌了嗎?
10
有研究者對於MDMA造成神經毒性的證據提出質疑。
從實驗動物的研究中,發現MDMA對血清素系統的神經細胞造成上述的三項變化,並推斷這些變化會造成神經功能的長期損害。然而,這三項神經細胞的變化意義都受到挑戰:
1. 血清素與血清素之代謝物5-HIAA濃度下降、合成血清素的酵素功能下降
這些細胞內的變化雖然會持續一段時間,但血清素的合成和濃度值終究會恢復到正常狀態,而非長期的匱乏和功能失效。此外,有研究顯示即便在高劑量MDMA的作用下,神經細胞內的血清素一般會下降40至60%,但細胞外的血清素濃度仍會維持與一般情形相同,使得細胞間的訊息傳遞仍可有足夠的血清素維持運作。研究者透過動物實驗發現MDMA的使用會產生長期的代償機制,包括減少血清素傳輸器回收血清素的能力、降低血清素的代謝以及降低血清素神經細胞釋放血清素的能力這三項功能,來維持大腦血清素系統的運作。並且,這些變化只能算是神經細胞內的成份變化,並不能視為是神經細胞結構受到了破壞。
也有不少研究對實驗動物(包括常用的老鼠和靈長類動物)進行一些學習、記憶的行為功能測試,來確認是否MDMA引發神經細胞內血清素的大量消耗會造成實驗動物的行為異常,藉此企圖來證明人類的MDMA使用者身上所觀察到長期認知功能的損害與MDMA有關(請看下面段落的討論)。然而這些研究無法有確切的證據證明其關聯性,研究者推測可能的原因包括血清素濃度的下降程度尚不足以造成認知功能的影響,因為如上一段所述的代償機制可以彌補神經細胞內血清素的不足來維持細胞外的血清素濃度;也有可能是大腦整體的功能可以去代償血清素系統功能的減損,維持住正常的行為能力;而若MDMA真的會造成實驗動物的行為影響,可能是行為的變化太過細微和隱性,測驗項目無法偵測出來。
2. 分泌血清素的神經細胞軸突末端上,血清素傳輸器的量減少、回收血清素的量也減少
有人類的腦度影像學研究顯示,若停止使用Ecstasy,血清素傳輸器的數量會再恢復到與原來的數目沒有差異的程度,因此變化是可逆的而非永久的。另一方面,一些新型的抗憂鬱劑―例如選擇性血清素回收抑制藥物(Selective serotonin reuptake inhibitor, SSRI) ―便是作用在血清素傳輸器上,抑制血清素的回收而能產生抗憂鬱的療效,而長期使用這類藥物也會造成血清素傳輸器的數量下降。抗憂鬱劑雖然會對神經細胞造成這些變化,但實際能帶來治療效果,那麼推斷MDMA造成神經細胞上的血清素傳輸器減少是一種傷害性的變化,應該要有更多證據。
另外,過去有一種食慾抑制劑fenfluramine也會促成神經細胞內的血清素消耗以及血清素傳輸器數量的減少,作用與MDMA非常相近,但是fenfluramine在長達24年的上市時間,並沒有報告指出會對人類的認知功能產生負面的影響(最後下架的原因是疑似會對心臟瓣膜造成損害),因此也讓人懷疑以上兩種所謂神經毒性的表現特徵,是否真的是造成認知功能損害的病因。也有人類的腦部影像學研究指出,雖然Ecstasy使用者在停用Ecstasy之後血清素傳輸器的數量會恢復,但是認知功能的損害仍會持續,也成為質疑上述假說的合理性。
3. 分泌血清素的神經細胞,其較末端的軸突數量會減損,留存的軸突則會出現腫脹和破裂化,稍後增
生的軸突也與原先之神經結構不同
MDMA對神經細胞結構上的改變,僅限於較末端的軸突,對較靠近細胞本體的軸突以及細胞本體則無影響,而神經細胞周邊也沒有典型神經細胞受到破壞後會出現的組織學變化,因此較為貼切的說法應稱作「去軸突化(axotomy)」,而非對整個神經細胞的傷害。加上末端的軸突經過一段時間之後亦會再生、重新與其他神經細胞接合(雖然不見得會完全恢復成原來的連接結構),因此有研究者認為MDMA尚未達到神經細胞結構的破壞之程度。
有研究進一步利用電生理偵測儀器觀察使用過MDMA的實驗動物之血清素神經細胞的功能,發現MDMA並沒有使能夠運作的神經細胞數量減少,神經細胞的功能也並無異常。
此外,也有研究發現使用高劑量的SSRI類抗憂鬱劑也會產生類似MDMA對神經細胞軸突的改變,所以這樣的軸突改變究竟會引發什麼效果,仍有待釐清。
總而言之,三項神經細胞在結構、功能上的變化要被認定已達到產生「神經毒性」的程度或許並不貼切,因為並未產生顯著、永久、不可逆的細胞傷害,或許稱MDMA具有「神經調節作用(neuroadaptation或neuromodulation)」會更為恰當。
11
那麼我們能夠將動物實驗研究上所發現的「神經毒性」,推導到人類身上也會產生嗎?
首先我們要先注意到的是,動物實驗使用的是高劑量的MDMA,至少10毫克/每公斤,並且在短時間內重複多次給予MDMA,才會造成實驗動物的神經毒性。然而人類使用的Ecstasy,一顆含有MDMA的量一般會在60到120毫克之間,因此若一位60公斤的人,服用一顆Ecstasy的話劑量等於1到2毫克/每公斤;而Ecstasy使用者,一次的使用量一般會在1到3顆之間,會極高量、多次重複使用Ecstasy的人還是占極少數。因此動物實驗的MDMA使用模式,和一般的Ecstasy使用習慣來說,是有著不小的差距,這對於我們要將動物實驗的結果「轉譯(translate)」到人類實際使用Ecstasy的效果上,有著不容忽視的重要性。
在這邊要先插入一個提問:科學研究除了要去證明MDMA是否會造成神經毒性,是否有想要去發現「究竟MDMA的使用量要達到多少才會造成神經毒性」?如果研究能夠去找出一個臨界值的範圍,是否就能夠以此證據來鼓勵Ecstasy的使用者,將Ecstasy的使用量控制在一定數量下,以減少MDMA可能帶來的傷害性?又或者,MDMA的使用也能在確保安全性的前提下,來發掘其治療的潛力?然而,在「向毒品宣戰」政策的執行下,藥物的使用應全面被禁止,不容許有灰色地帶存在,這樣的思考必然會遭受到打壓。
過去動物實驗的研究者,對於如何將動物實驗中產生某一反應的MDMA使用劑量轉換成為人類產生相同反應的使用劑量有一套算法。因為體型小的動物其基礎代謝率較高,因此可以承受較高劑量的藥物在體內並快速將之代謝,經由一計算公式的換算,實驗老鼠使用5毫克/每公斤的MDMA效果會等於人類使用70毫克的MDMA(約1毫克/每公斤)。
然而這樣的換算方式被批評為過於簡化,因為並沒有考量到「藥物動力學(pharmacokinetics)」的因素。藥物動力學指的是藥物進入體內後的吸收、分佈、代謝和排除,而不同物種間的藥物動力學可能存在極大的差距,因此原先換算公式中預估具有同等效果的兩個不同MDMA劑量,在分別進入實驗老鼠和人類體內,經過吸收、分佈的過程而最終進入到大腦的藥物濃度―評估藥物產生的效應和副作用的最精確指標―便會有差異;而MDMA在實驗動物和人體內代謝過程的不同―因為神經的傷害是來自於MDMA代謝物的作用―也將導致神經傷害性的不同程度。此外,動物實驗大多是經由腹腔或皮下注射MDMA,而非人類大多口服的方式,不同的攝入方式也將造成藥物在體內累積的速度、最高濃度高低的差異,要直接進行比較也會有誤差因此若沒有考量到藥物動力學,那麼企圖將動物實驗的結果轉譯到人類上便會不精確。
舉一些實際例子來說,MDMA在人體會經由肝臟酵素CYP2D6進行代謝成為HHMA,但是MDMA本身會去抑制CYP2D6的功能,使得代謝速度減緩、MDMA得以累積不被代謝而讓濃度升高,因此若使用的MDMA愈多,造成愈多CYP2D6被抑制,便會讓MDMA濃度升高得更快。研究顯示,當使用的MDMA從1毫克/每公斤加倍到2毫克/每公斤,血液中的MDMA濃度卻會以非線性的方式增加到4倍。人類的如此特性便可能與其他實驗動物不同,而讓血中MDMA濃度的變化有差異。
此外,人體內的MDMA除了被CYP2D6代謝,還會被另一種肝臟酵素CYP3A4代謝成為MDA,而MDA造成神經傷害的所需濃度比MDMA還來得低,因此更容易造成神經的傷害性。人類跟實驗老鼠相較之下,MDMA被轉換成MDA的比例較低(10% vs 23-34%),因此MDMA在人體內對神經的影響性較實驗老鼠體內來得小。
另外,實驗發現MDMA在人體內到達最高濃度的時間以及被代謝到剩下一半濃度的時間都相較實驗動物來得長,因此有研究者認為,由於MDMA在人體內的代謝速度較為緩慢,讓MDMA的代謝物(具有神經傷害性)生成速度較慢,可以讓體內去抵銷MDMA代謝物作用的保護機制充分地化解神經細胞被傷害的機會;而實驗動物快速地進行MDMA的代謝,反倒讓MDMA代謝物快速生成、濃度升高,增加了神經傷害的風險。
圖片三:左欄是人類口服MDMA後的數據,中間和右欄是實驗老鼠口服和腹腔注射MDMA的數據。Tmax指的是
MDMA在血液中到達最高濃度所需的時間,t1/2指的是MDMA被代謝到剩下最高濃度一半時所需的時
間。我們可以看到MDMA在人類體內要達到Tmax和t1/2的時間都比實驗老鼠來得慢。
( 圖片來源:Green AR, King MV, Shortall SE, Fone KC. Lost in translation: preclinical studies on 3,4-
methylenedioxymethamphetamine provide information on mechanisms of action, but do not allow
accurate prediction of adverse events in humans. Br J Pharmacol. 2012 Jul;166(5):1523-36. )
要讓實驗動物如老鼠和猴子產生神經的傷害,必須接受多次高劑量的MDMA才能達致,而高劑量的MDMA在實驗動物體內的血液濃度可高達2000ng/ml,但因為實驗動物能夠快速代謝MDMA,因此動物可以承受極高的MDMA濃度而不至於被MDMA的急性副作用(主要為體溫過高及相關併發症)所傷害;然而人類對MDMA的代謝速度慢,因此人類要產生嚴重的急性副作用所需的MDMA濃度要低許多,有紀錄顯示在1000-1500 ng/ml。因此有研究者從藥理學觀點大膽推斷,人類使用MDMA是不會造成神經傷害的,因為人類若嘗試使用足以造成神經傷害的MDMA劑量,可能先因為急性副作用而死亡,而即便得以生存,因為高劑量的MDMA會抑制CYP2D6的功能,緩慢的MDMA代謝也能防止神經的傷害;至於一般Ecstasy使用者所使用的藥物劑量很少會使用到產生嚴重的急性副作用,因此更不可能產生神經傷害的效果。
總的來說,以目前現有的動物實驗結果,雖然可以證實MDMA對實驗動物會造成神經的影響性(但是否可稱作神經毒性則仍有爭議),但在缺乏MDMA在實驗動物和人類體內的完整藥物動力學資訊下,要推導出人類究竟需要多少使用量才會對神經造成影響,以目前的證據來說仍嫌不足,自然也無法確認一般娛樂性使用MDMA的狀況下對神經的影響性。不過我們可以發現將藥物動力學的一些因素考量進去的話,可以發現MDMA對人類的神經影響性可能比實驗動物來得小,這在將動物實驗結果轉譯到人類身上時必須要特別小心。
12
那麼人類的研究也有問題嗎?
前面有提過,因為MDMA直接使用在人體上進行研究被認為可能造成神經毒性,因此在不違反研究倫理之下,不進行主動給予人體試驗者MDMA的前驅性(prospective)的研究(將MDMA實際用在人體上的研究是較為晚近的事,請看下面之段落),而選擇回溯性(retrospective)的研究法來回顧是否Ecstasy的使用者會受到不良影響。然而這樣的研究方法具有很多瑕疵,使得證據的可信度大大受到影響。
首先最關鍵的是,研究調查的是Ecstasy的使用者,但是Ecstasy畢竟不是MDMA,Ecstasy的製造者可能合成出純度不夠的MDMA,或是加入其他成分來稀釋、替代MDMA,使得研究者或使用者無從得知每一顆被服下的Ecstasy中究竟有多少含量的MDMA,甚至究竟是否含有MDMA。在無法定性、定量的情況下,研究所得到人體大腦受到影響的證據,僅能說是與Ecstasy有關,但無法充分以「這是MDMA所造成的」來做解釋,也無法確知究竟多少量的MDMA會造成影響。
其次,研究要將試驗者進行分組,讓各組之間的變因只有是否使用Ecstasy,把其他變因(例如年紀、性別、族群、居住地、學歷、智商、社經地位等等)都控制住來進行分析,才能判斷是否Ecstasy使用會造成認知功能的異常。然而,由於Ecstasy使用者大多隸屬於音樂次文化的社群,在生活型態(例如經常徹夜不眠參加派對、大量消耗體力)、藥物使用(較為多樣化的藥物使用)等等變因的存在下,都有可能會對認知功能造成影響,若在選擇試驗者時沒有考量到這些變因的話,便會導致變因未受到控制而讓分析出現瑕疵。
第三,請Ecstasy使用者回溯性地自述自己的藥物使用量,很可能會出現報告使用的數量、頻率的不精確之問題,而使用者也可能會誇大或少報自己的使用量,都讓資訊收集的品質下降。況且,若使用各式藥物可能造成記憶力的損害―如研究認為血清素系統受到破壞會造成記憶力的缺損―那使用者回報的資訊更有可能出現偏差。
第四,另一個影響研究結果很重要的是,Ecstasy的使用者也多數是其他藥物的使用者,包括安非他命、古柯鹼、大麻、迷幻藥、K他命、鎮定劑等等,長期地使用各種藥物都可能造成認知功能的影響。例如大麻在持續使用的狀況下會造成認知功能的缺損,但長期戒除後會恢復;而安非他命雖然主要會對大腦的多巴胺系統造成損害,但對血清素系統也會造成影響,若研究認為認知功能的缺損與血清素有關,那安非他命的影響性也不容忽視。早期許多研究並沒有將其他藥物的因素考量進去,在沒有將這些變因控制住的情形下,因此絕大多數的研究都傾向於將認知功能的缺損歸咎於Ecstasy (MDMA)上;即便後來將這個問題進行修正,但是研究的結果也並非全部支持Ecstasy (MDMA)會造成影響,例如有研究企圖找尋認知功能缺損與大麻或Ecstasy的關係,有的研究發現與大麻有相關性,有的研究則認為與Ecstasy有相關性,使得要直接將認知功能缺損歸因於MDMA證據仍不足。
第五,許多會與Ecstasy合併使用的藥物,或者是參雜在Ecstasy裡頭的各種不為使用者和研究者所知的成份,都可能會經過與MDMA的交互作用後造成MDMA的藥物動力學改變,或是影響MDMA的作用機轉,而讓MDMA對神經影響性的升高,例如有研究發現合併酒精的使用會升高MDMA的濃度。但關於藥物交互作用的研究並不多,使得要識別出交互作用的影響性仍相當不足。
第六,研究發現Ecstasy的使用者會在認知功能、情緒、焦慮度和衝動性等方面較為脆弱,並推論是因為使用Ecstasy造成血清素系統功能損害所導致。然而這樣的推導忽略了一個可能性,會不會是這些人本身的血清素系統功能就比較脆弱,而有這些精神病理的問題,才導致藥物的濫用,而不是使用Ecstasy的結果?然而回溯性的研究無法進行分辨,因為無法在Ecstasy使用者尚未使用藥物前進行測驗,來判斷是否這些使用者本身就擁有血清素系統較脆弱的特質。
綜上所述,以回溯性的研究方法要去分析MDMA是否會造成人類的認知功能損害,存在著許多的研究瑕疵,增加了要去釐清MDMA真正效力和影響力的阻礙。唯有在周全地控制變因、給予試驗者服用純的MDMA、在使用MDMA前後進行完整的評估和檢測以進行比較的前驅性研究,才有可能真正判斷出MDMA是否具有神經毒性。但是在全面禁毒的政策大纛下,人類的研究比動物實驗要晚了數年之久才開始跨出第一步,而且也無法實際進行研究去探測出可能造成神經毒性的臨界值。
還有一個問題是,大多數的研究都企圖去確認「使用Ecstasy會不會造成認知功能損害」,而在一個不理想的研究方法下,總和的研究結果傾向於認定使用Ecstasy會對認知功能造成影響。但是Ecstasy使用者的藥物使用量、頻率差異相當大,有的是偶爾一為之,有的則是頻繁使用,有的是一次就服下大量Ecstasy,有的才剛開始使用,有的則已經使用十年以上。不同的使用型態或許會對認知功能的影響有差異,就如同有動物實驗顯示使用較低劑量和頻率的MDMA並不會造成神經的異常變化,而確實有少數將Ecstasy使用者劃分為輕、中、重度使用者(不同研究之定義不一)的研究發現,若有出現認知功能缺損會集中在重度使用者的族群中。如果MDMA的使用真的會造成人類神經的傷害,那麼研究若能鑑別出MDMA在什麼程度的使用下不會造成認知功能的影響,而不再只是得出黑白分明的「是或否」答案,那對於Ecstasy使用者來說,是不是就能夠依循這個參考意見來減低個人認知功能的損害風險?
訂閱:
張貼留言 (Atom)


沒有留言:
張貼留言